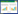扩展功能
文章信息
- 周冠宇, 李江华, 彭政, 苗周迪, 冒鑫哲, 张娟
- ZHOU Guanyu, LI Jianghua, PENG Zheng, MIAO Zhoudi, MAO Xinzhe, ZHANG Juan
- 定点突变提高枯草芽孢杆菌角蛋白酶的低温催化活性
- Improving the low-temperature activity of Bacillus subtilis keratinase by site-directed mutagenesis
- 微生物学通报, 2022, 49(1): 1-13
- Microbiology China, 2022, 49(1): 1-13
- DOI: 10.13344/j.microbiol.china.210748
-
文章历史
- 收稿日期: 2021-08-16
- 接受日期: 2021-09-17
- 网络首发日期: 2021-10-27
2. 江南大学生物工程学院,江苏 无锡 214122;
3. 江南大学未来食品科学中心,江苏 无锡 214122
2. School of Biotechnology, Jiangnan University, Wuxi 214122, Jiangsu, China;
3. Science Center for Future Foods, Jiangnan University, Wuxi 214122, Jiangsu, China
角蛋白是一种不溶性且含硫量高的丝状蛋白,广泛分布于动物表皮附属物(如毛发、指甲、爪、龟甲、角、喙和羽毛)中[1]。由于半胱氨酸和甘氨酸含量很高,角蛋白非常坚韧,其在水中的溶解度低且难以降解[2]。常用的化学法和物理法处理角蛋白会不可避免地涉及高温、微波和强酸或强碱工艺,这不仅会造成巨大的能量消耗,还会对环境造成负担[3]。角蛋白酶是一种可以特异性降解角蛋白的水解酶,由土壤、水和各种富含角蛋白的来源中发现的不同类型微生物分泌[2]。随着可持续性和绿色概念的兴起,角蛋白酶在工业生产与实际应用中的潜力逐渐被挖掘出来[4],其在制革[5]、化妆品[6]、饲料[7]等多个行业中都被认为是一种能改善现有工艺的重要生物酶。
我们课题组在前期工作中得到的角蛋白酶KerZ1属于角蛋白酶S8家族[2],其在60 ℃的最适反应温度下可以高效水解角蛋白底物[8]。然而过高的最适温度可能并不适合如皮革加工、化妆品使用等实际环境。此外,冷适应的酶由于其在中等和更低温度下具有更高的活性,不仅能有效减少工业生产中昂贵的加热成本,限制不必要的化学副反应对产品造成的不良影响,其热不稳定的特性还可以用于在生产中根据工艺步骤进行选择性的灭活,因而在实际应用中有着巨大的潜力[9]。因此,对角蛋白酶KerZ1的低温催化活性改造能大幅提高其应用价值。
与热适应的同源酶相比,嗜冷酶在低温下通常具有更高的构象灵活性,具体原因包括但不限于甘氨酸和赖氨酸残基数量增加、脯氨酸和精氨酸残基频率降低、疏水核心减少、表面疏水性增加和氢键减少等[10]。然而灵活的蛋白质结构意味着分子刚性较低,这会导致酶热稳定性的下降,所以对嗜热酶的低温催化活性改造过程中通常需要在低温催化活性与热稳定性之间进行权衡[11]。由于氨基酸取代和相互作用的复杂性及许多情况下无法正确解释所选随机突变的影响,因此,与成熟的热稳定性改造策略相比,目前对酶的低温催化活性进行改造仍具有挑战性[12]。一直以来对酶的低温催化活性改造策略以定向进化为主[13-16]。最近一些新的策略被相继提出,例如:通过不稳定化酶-辅酶-底物三元复合体来降低酶促反应过渡态需要的能量,使酶促反应更易逾越能量壁垒,从而提高酶在低温下的催化效率[17]; 通过向酶分子引入额外盐桥从而同时增加末端刚性和催化结构域柔性来提升低温催化活性[18]等。柔性环区域(loop)是蛋白质结构中最灵活的区域,是调节酶催化活性、稳定性、底物特异性的重要区域,也是提高酶分子低温催化活性的潜在目标。例如对嗜热脂肪酶A的loop区进行饱和突变来筛选嗜冷酶突变体,这些突变体在低温条件下的分子动力学模拟结果均显示出更高的灵活性[19]。因此,对酶分子loop区柔性改造策略的可行性已得到证实。基于这些假设,我们通过同源比对和计算辅助方法向高温角蛋白酶KerZ1柔性环区域引入氨基酸突变,以期提升其中温及低温催化活性,并试图提升其在工业生产和实际应用场景中的性能。
1 材料与方法 1.1 材料 1.1.1 菌株和质粒研究所用质粒pP43NMK、pP43NMK-KerZ1及宿主枯草芽孢杆菌(Bacillus subtilis) WB600由本实验室前期构建保存,大肠杆菌感受态细胞E. coli JM109 Competent Cells购自宝生物工程(大连)有限公司。
1.1.2 主要试剂和仪器PrimeSTAR® Max DNA Polymerase和Dpn I,宝生物工程(大连)有限公司; Bradford试剂盒,生工生物工程(上海)股份有限公司; HisTrap™ HP预装柱,GE Healthcare公司; 角蛋白(部分磺化,5%于水中),梯希爱(上海)化成工业发展有限公司。PCR仪,Bio-Rad公司; 振荡恒温金属浴,Bioer公司; 酶标仪,BioTek公司; 紫外分光光度计,Shimadzu公司。
1.1.3 PCR引物设计研究中的引物合成与DNA测序通过生工生物工程(上海)股份有限公司完成,使用的引物见表 1。
| 引物名称Primers name | 序列Sequence (5′→3′) |
| F21Y-F | AAGTGCAGGCTCAAGGCTATAAGGGAGCGAATGTAAAAGTAGCCG |
| F21Y-R | AGCCTTGAGCCTGCACTTTGT |
| Q36H-F | CTGGATACAGGAATCCACGCTTCTCATCCGGACTTGAACGTAG |
| Q36H-R | TGGATTCCTGTATCCAGGACGGC |
| N61Q-F | GCTTATAACACCGACGGCCAAGGACACGGCACACATGTTGC |
| N61Q-R | GCCGTCGGTGTTATAAGCTTCG |
| T161S-F | AGCGGATCTTCAGGAAACTCGAATACAATTGGCTATCCTGCGAAATACG |
| T161S-R | GTTTCCTGAAGATCCGCTGTTCCC |
| N162S-F | GGATCTTCAGGAAACACGAGTACAATTGGCTATCCTGCGAAATACGAT |
| N162S-R | CGTGTTTCCTGAAGATCCGCTG |
| I164V-F | TCAGGAAACACGAATACAGTTGGCTATCCTGCGAAATACGATTCTGTC |
| I164V-R | TGTATTCGTGTTTCCTGAAGATCCGCT |
| V173T-F | CCTGCGAAATACGATTCTACCATCGCTGTTGGTGCGGTAGAC |
| V173T-R | AGAATCGTATTTCGCAGGATAGCCAAT |
| F188S-F | AACAGCAACAGAGCTTCATCTTCCAGTGTGGGAGCAGAGCTT |
| F188S-R | ATGAAGCTCTGTTGCTGTTAGAGTCTAC |
| G203S-F | ATGGCTCCTGGCGCAAGCGTATACAGCACTTACCCAACGAACACT |
| G203S-R | TGCGCCAGGAGCCATGAC |
| T210S-F | GTATACAGCACTTACCCAAGCAACACTTATGCAACATTGAACGGAACG |
| T210S-R | TGGGTAAGTGCTGTATACGCCTG |
| N211S-F | TACAGCACTTACCCAACGAGCACTTATGCAACATTGAACGGAACGTC |
| N211S-R | CGTTGGGTAAGTGCTGTATACGC |
| T212G-F | AGCACTTACCCAACGAACGGTTATGCAACATTGAACGGAACGTCAATGG |
| T212G-R | GTTCGTTGGGTAAGTGCTGTATACGC |
| Y255P-F | TCCAGCACGGCGACTCCTTTGGGAAGCTCCTTCTACTATGGGAAAGG |
| Y255P-R | AGTCGCCGTGCTGGAG |
| T210S/N211S/T212G-F | GTATACAGCACTTACCCAAGCAGCGGTTATGCAACATTGAACGGAACGTCAATGG |
| T210S/N211S/T212G-R | TGGGTAAGTGCTGTATACGCCTGC |
| 注:加下划线的碱基为替换的密码子 Note: The underlined base is the replacement codon. | |
LB培养基(g/L):酵母粉5.0,蛋白胨10.0,氯化钠10.0。固体培养基需要额外添加20.0 g/L琼脂粉,1×105 Pa灭菌15 min。
发酵培养基(g/L):蔗糖30.0,蛋白胨20.0,酵母粉10.0,Na2HPO412H2O 6.0,KH2PO4 3.0,MgSO47H2O 0.3。1×105 Pa灭菌15 min。
重组大肠杆菌的筛选和培养使用LB培养基(含100 μg/mL氨苄青霉素),培养条件为37 ℃,摇床转速为220 r/min,培养12 h; 重组枯草芽孢杆菌的筛选和培养使用LB培养基(含50 μg/mL卡那霉素),培养条件为37 ℃,摇床转速为220 r/min,培养12 h; 重组枯草芽孢杆菌的发酵使用发酵培养基(含50 μg/mL卡那霉素),培养条件为37 ℃,摇床转速为220 r/min,培养24 h。
1.2 角蛋白酶的三维结构模拟角蛋白酶KerZ1氨基酸序列通过氨基酸翻译软件获得,利用在线服务器SWISS-MODEL (https://swissmodel.expasy.org/)搜索模板,以与角蛋白酶KerZ1氨基酸序列具有99.63%相似性的丝氨酸蛋白酶KerA与抑制剂Greglin复合体(PDB 4gi3,X-RAY DIFFRACTION 1.75 Å)为模板建立同源模型[20],并使用Molprobity在线模型分析工具(http://molprobity.biochem.duke.edu/index.php)对模型质量进行检测。
1.3 角蛋白酶突变体的构建对角蛋白酶突变位点进行全质粒PCR扩增[21],PCR产物经过Dpn I酶切消化后转化大肠杆菌感受态细胞,转化产物涂布LB固体培养基。37 ℃培养过夜后从LB平板上挑选转化子进行菌落PCR验证,挑选验证正确的阳性转化子提取质粒送样测序,将测序正确的重组质粒转化表达载体B. subtilis WB600,转化产物涂布LB固体培养基,37 ℃培养过夜后得到的转化子即为表达目标角蛋白酶突变体的重组菌。
1.4 角蛋白酶突变体的表达及纯化将重组枯草芽孢杆菌接种至LB培养基中,于37 ℃培养过夜作为种子液,取1 mL接种于50 mL发酵培养基中进行发酵。将获得的菌液于4 ℃、7 000 r/min离心20 min,所得的上清液即为粗酶液。使用0.22 μm水系滤膜对粗酶液进行抽滤后使用HisTrap™ HP预装柱纯化角蛋白酶。首先使用缓冲液A (含20 mmol/L pH 7.4的Tris-HCl缓冲液)平衡纯化柱,以2 mL/min流速上样30 mL,随后使用缓冲液B (含500 mmol/L咪唑,20 mmol/L pH 7.4的Tris-HCl缓冲液)取代角蛋白酶,10%分离缓冲液B等度洗脱置换出目的蛋白。使用SDS-PAGE与Bradford蛋白定量试剂盒检测酶液的纯度与蛋白浓度。
1.5 角蛋白酶酶活的测定将酶液进行适当稀释使得反应体系显色后OD660在0.1−1.0范围内,以150 μL pH 10.0的50 mmol/L Gly-NaOH溶液作为缓冲液,100 μL 25 g/L的可溶性角蛋白作为底物,加入50 μL稀释的酶液,混匀后于60 ℃反应20 min; 反应结束后立即加入200 μL的0.5 mol/L三氯乙酸终止反应,并于12 000 r/min离心2 min。随后取200 μL反应液加入到1 mL 50 g/L的Na2CO3溶液中,再加入200 μL福林酚试剂混匀后于50 ℃显色10 min,以加入底物前先加入三氯乙酸终止反应但其他操作相同的反应体系作为空白对照,使用分光光度计于OD660测定吸光度。酶活单位定义为:1个活力单位(U)为吸光度在OD660下升高0.001单位[22]。
1.6 角蛋白酶酶学性质的测定最适反应温度(Topt)的测定:将酶活测定反应温度更改为20、30、40、50、60、70、80 ℃,其余条件不变,对纯化后的角蛋白酶KerZ1及其突变体进行酶活测定。以各个酶最高酶活作为100%,其余温度为相对酶活,绘制反应温度-相对酶活曲线,并计算在不同温度条件下各角蛋白酶的比酶活。
半衰期(t1/2)的测定:将经过纯化的角蛋白酶KerZ1及其突变体酶置于60 ℃金属浴中保温,每10 min取样并进行酶活测定。以保温处理前酶活作为100%,之后每次取样点的酶活为相对酶活。绘制以残余酶活的ln值为纵坐标、保温时间t为横坐标的散点图,对各个数据点进行线性拟合以计算角蛋白酶失活速率常数k,带入公式t1/2=ln2/k以计算各个角蛋白酶半衰期[23]。
反应动力学参数的测定:将可溶性角蛋白底物稀释成不同质量浓度(0、2、4、6、8、10、12 g/L),将角蛋白酶酶液进行适当稀释使得反应体系显色后OD660在0.1–1.0范围内,测定角蛋白酶KerZ1及其突变体在不同底物浓度下的反应初速,以底物浓度和反应速率绘制散点图,运用Origin 2021对各个数据点使用米氏方程进行非线性拟合直至收敛,得到最大反应速率(Vmax)和米氏常数(Km),并进一步计算催化常数kcat及催化效率kcat/Km。
1.7 分子动力学模拟使用AMBER16对角蛋白酶KerZ1及其突变体进行分子动力学模拟,添加力场ff14SB,添加水分子盒子包裹蛋白质模型,设定蛋白质表面到水盒子边界的最小距离为12 Å,平衡系统设定为150 mmol/L的氯化钠,分子动力学模拟参数包括能量最小化、50 ps的0−300 K的升温过程、500 ps的平衡过程和20 ns的动力学模拟[21]。使用AMBER16分析氨基酸残基的均方根浮动(root mean square fluctuation,RMSF)。
2 结果与分析 2.1 角蛋白酶低温催化活性单点突变位点的选择同源比对常用于酶分子改造中关键突变位点的确定。以角蛋白酶KerZ1的氨基酸序列为模板,从文献中挖掘了2株最适反应温度在40 ℃的角蛋白酶氨基酸序列,利用ClustalX 2.1和Esprint 3.0对角蛋白酶KerZ1及挖掘的同源序列进行比对和分析[5, 24]。同时使用PyMOL软件对建立的角蛋白酶KerZ1同源模型(PDB 4gi3)中的loop区进行标注,结果如图 1所示。我们向每个loop区引入相应的氨基酸单点突变以提升其结构灵活性。然而,根据同源比对结果有大量的突变位点可供选择,进一步确定要引入的突变位点需要借助计算机辅助筛选。利用Discovery Studio对引入的氨基酸突变进行模拟,计算突变角蛋白酶的折叠自由能变化(ΔΔG),其结果如表 2所示。折叠自由能(ΔG)是蛋白质从折叠态到伸展态间的吉布斯自由能差,受氢键、范德华力、熵效应等因素的综合影响,是最重要的蛋白质热力学参数之一,也是反映蛋白质结构刚性的重要指标[25]。一般认为,蛋白质的ΔG越低,其具有的结构刚性就越强。因此,在许多研究中都使用了生物信息学方法对蛋白质进行模拟突变,并通过得到的ΔΔG来预测该突变对蛋白质结构刚性的影响,从而指导蛋白质热稳定性的改造[26]。本研究的目的在于通过突变得到一株在中等和较低温度下仍保留较高酶活的角蛋白酶突变体,因而更倾向于选择折叠自由能提升(即ΔΔG > 0)的突变位点,意味着引入的氨基酸突变会使突变体相较原始酶的灵活度更高,这是提升低温催化活性所必需的。基于上述理论,我们引入了共计13个单点突变对8个loop区进行柔性改造,分别为F21Y、Q36H、N61Q、T161S、N162S、I164V、V173T、F188S、G203S、T210S、N211S、T212G、Y255P。
|
| 图 1 不同来源角蛋白酶氨基酸序列对比 Figure 1 Comparison of amino acid sequences of keratinase from different sources. |
|
|
| 柔性环区域Loop | 引入的模拟氨基酸突变Simulated amino acid mutations | 折叠自由能变化ΔΔG (kcal/mol) |
| Loop 2 | F21Y | 0.23 |
| Loop 3 | Q36H | 1.51 |
| Loop 4 | A52P | −0.69 |
| G53S | 0.00 | |
| N61Q | 0.88 | |
| Loop 5 | T78I | −0.47 |
| Loop 6 | S102Q | −0.27 |
| Loop 7 | G117N | −0.55 |
| Loop 8 | A128P | −0.49 |
| Loop 10 | N160S | −1.03 |
| N160F | −0.47 | |
| T161S | 0.33 | |
| N162S | 1.71 | |
| I164V | 1.48 | |
| V173T | 0.16 | |
| Loop 11 | S183N | −0.54 |
| N184V | −0.50 | |
| F188S | 2.55 | |
| Loop 12 | A202T | −0.23 |
| G203S | 0.16 | |
| Loop 13 | T210S | 0.19 |
| N211S | 0.23 | |
| T212G | 1.43 | |
| Loop 14 | S241T | −0.43 |
| Loop 15 | Y255P | 1.82 |
| S258D | −0.33 |
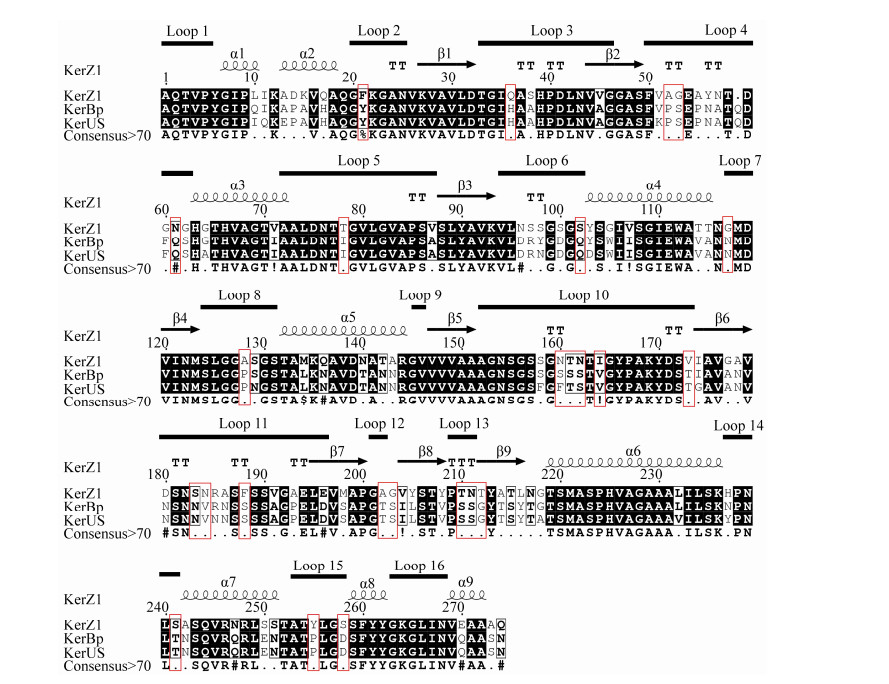
通过全质粒PCR扩增将突变氨基酸引入pP43NMK-KerZ1为模板,将测序正确的质粒转化到B. subtilis WB600中,摇瓶发酵表达角蛋白酶KerZ1及其突变体。在40 ℃反应条件下测定角蛋白酶粗酶液的酶活,结果如图 2所示。在loop 13引入的突变体T210S、N211S、T212G对角蛋白酶在较低温度下的酶活,相比野生型角蛋白酶KerZ1均有显著的提升,这说明原始酶可能在该loop区的整体结构灵活性不佳,对该loop区的改造易提升其柔性; 与之相反,在loop 10引入的突变体N161S、N162S、I164V、V173T均显示出显著且不同程度的活性下降,则说明原始酶可能在该loop区的灵活性较高,不适宜进行进一步的柔性改造。基于这个假设对loop 13进行了复合突变,构建了角蛋白酶KerZ1复合突变体T210S/N211S/T212G。经过24 h的摇瓶发酵,突变体T210S/N211S/T212G粗酶液在40 ℃的酶活达到了63.17±3.25 kU/mL,相较于作为对照的角蛋白酶KerZ1的40.60±0.60 kU/mL提升了55.59%,其在低于最适温度条件下的酶活得到了显著提高。
|
| 图 2 角蛋白酶突变体在40 ℃反应条件下的酶活 Figure 2 Enzyme activity of keratinase mutants at 40 ℃. |
|
|
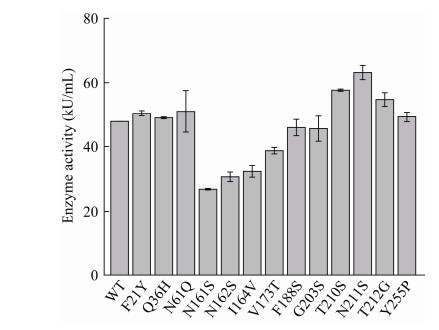
通过镍离子亲和色谱柱对角蛋白酶KerZ1和突变体T210S、N211S、T212G及其复合突变T210S/N211S/T212G的发酵粗酶液进行纯化,并进行SDS-PAGE电泳分析,结果如图 3所示,角蛋白酶KerZ1及其突变体的分子量约为28 kDa。将得到的纯酶液用于进一步的酶学性质分析。
|
| 图 3 KerZ1及其突变体的SDS-PAGE电泳分析 Figure 3 SDS-PAGE analysis of KerZ1 and mutant enzymes. M:蛋白质标准分子质量; 1−5:KerZ1、T210S/N211S/T212G、T210S、N211S、T212G纯酶液 M: Protein marker; 1−5: KerZ1, T210S/N211S/T212G, T210S, N211S, T212G. |
|
|
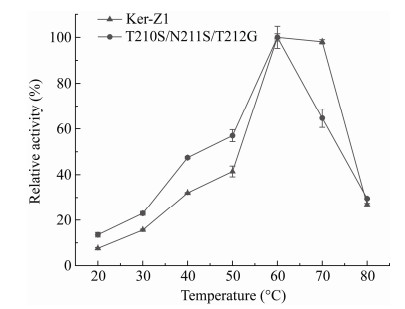
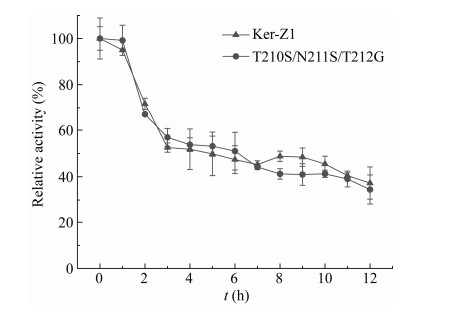
对角蛋白酶KerZ1及突变体的酶学性质进行测定,结果如表 3所示。突变体的最适反应温度均为60 ℃,相较于KerZ1无变化。在最适温度条件下,突变体T210S/N211S/T212G的比酶活与KerZ1相比略微下降了1.66%,但在40 ℃的中等温度和20 ℃的低温条件下其比酶活相比KerZ1分别提升了45.68%和85.74%,单突变体T210S、N211S、T212G与KerZ1在低于最适温度条件下的比酶活也有不同程度的提高。为进一步探究突变体T210S/N211S/T212G在低于最适温度条件下的性能,绘制了其与KerZ1的温度依赖酶活曲线。从图 4可以看出,虽然最适温度并未降低,但该突变体的温度依赖酶活曲线相较于KerZ1有明显向低温偏移的趋势。低温催化活性的提升通常意味着分子柔性的提升,这会影响酶的热稳定性,突变体T210S/N211S/T212G、T210S、N211S和T212G的半衰期相比KerZ1分别降低了11.52%、16.02%、7.47%和31.23% (表 3),由于损失的热稳定性可能会影响突变体T210S/N211S/T212G在较低温度下的长期性能,因此在40 ℃时温浴角蛋白酶并测定其在该反应温度下的低温催化活性,以各酶保温处理前的酶活为100%绘制保温时间与各取样点残余酶活的曲线,如图 5所示。经过12 h的温浴,突变体T210S/N211S/T212G相比KerZ1并未显示出明显的低温催化活性损失,即该突变体的热稳定性损失对其在较低温度下的长期活性影响较小。综上所述,突变体T210S/N211S/T212G在不严重损失热稳定性的情况下其低温催化活性得到了显著的提高。
| 突变体 Mutant enzyme |
60 ℃时比酶活 Specific enzyme activity at 60 ℃ (kU/mg) |
40 ℃时比酶活 Specific enzyme activity at 40 ℃ (kU/mg) |
20 ℃时比酶活 Specific enzyme activity at 20 ℃ (kU/mg) |
Topt (℃) | t1/2 (min) |
| KerZ1 | 186.70±2.08 | 59.78±0.31 | 14.10±0.47 | 60 | 22.22±1.10 |
| T210S/N211S/T212G | 183.60±6.25 | 87.09±0.64 | 26.19±1.30 | 60 | 19.66±0.75 |
| T210S | 205.37±1.71 | 81.37±4.13 | 23.14±2.93 | 60 | 18.66±0.53 |
| N211S | 208.69±2.92 | 73.97±3.40 | 17.90±1.67 | 60 | 20.56±0.82 |
| T212G | 191.00±5.39 | 78.08±1.69 | 23.95±1.71 | 60 | 15.28±0.79 |
|
| 图 4 KerZ1及突变体T210S/N211S/T212G的温度依赖酶活 Figure 4 Temperature-dependent activity of KerZ1 and T210S/N211S/T212G. |
|
|
|
| 图 5 KerZ1及突变体T210S/N211S/T212G在40 ℃时的热稳定性 Figure 5 Thermostability of KerZ1 and T210S/N211S/T212G at 40 ℃. |
|
|
在40 ℃与60 ℃测定KerZ1及其突变体的反应动力学参数,结果如表 4所示。冷适应的酶常通过降低底物到产物之间的活化自由能壁垒使其在低温下具有更高的kcat值,与此同时,它们与底物的结合能力会略低于其嗜热的同源酶(具有更高的Km值),原因是这样可以用更低的能量促成酶分子与底物的复合[11]。虽然在60 ℃时突变体N211S与T210S/N211S/T212G的kcat值比KerZ1略低,但由于较低的Km使得其在最适反应温度下相比KerZ1仍具有较高的催化效率(更高的kcat/Km)。在40 ℃条件下,各突变体的Km及除突变体N211S外的kcat/Km与KerZ1相比均显示出不同程度的提升,其中T210S/N211S/T212G与KerZ1相比kcat/Km提高了35.89%,Km值提高了29.4%,符合冷适应的酶在较低温度条件下的反应动力学特征。结果表明,复合突变体T210S/N211S/T212G在低于最适反应温度的条件下虽然与底物的结合能力略低,但具有更高的催化效率。
| 突变体 Mutant enzyme |
Km (g/L) |
kcat (s−1) |
kcat/Km (L/(g∙s)) |
| 60 ℃ | |||
| KerZ1 | 1.52±0.14 | 192.67±2.52 | 126.91 |
| T210S/N211S/T212G | 1.22±0.13 | 165.77±1.52 | 135.40 |
| T210S | 1.75±0.18 | 207.66±4.87 | 118.63 |
| N211S | 1.11±0.19 | 168.02±7.35 | 151.38 |
| T212G | 1.78±0.18 | 212.97±5.13 | 119.39 |
| 40 ℃ | |||
| KerZ1 | 1.53±0.14 | 50.60±0.62 | 33.16 |
| T210S/N211S/T212G | 1.98±0.09 | 89.14±1.37 | 45.06 |
| T210S | 1.95±0.13 | 68.93±0.80 | 35.29 |
| N211S | 2.24±0.19 | 68.24±1.02 | 30.50 |
| T212G | 1.98±0.10 | 68.08±0.89 | 34.26 |
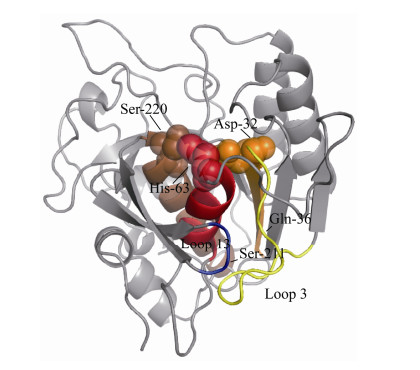
利用PyMOL对突变角蛋白酶分子结构进行模拟,并对loop 3与loop 13及活性位点的位置进行标注,如图 6所示。由于该角蛋白酶属于角蛋白酶S8家族,催化活性中心为其典型的催化三联体结构(32D-63H-220S,球形部分)[2]。不难发现,活性位点32D所在的β-折叠(橙色部分)与loop 3 (黄色部分)直接相连,而loop 13 (蓝色部分)及相邻的β-折叠也与活性位点220S所在的α-螺旋(棕色部分)紧密相连,因此推测loop 3及loop 13的结构灵活性会一定程度上影响活性位点32D及220S所在二级结构的灵活性。同时,loop 3、loop 13及其相邻的β-折叠与上述活性位点所在的α-螺旋及β-折叠组成的结构将活性位点63H所在的α-螺旋(红色部分)包裹于其中,推测该结构可能会限制催化三联体所在的3个二级结构之间的相对活动,而影响该结构整体灵活性的关键可能在于连接loop 3与loop 13的分子间作用力。因此,loop 3与loop 13之间作用力的变化可能会影响该结构的灵活性,进而影响角蛋白酶的低温催化活性。
|
| 图 6 Loop 3与Loop 13和活性位点在突变体T210S/N211S/T212G结构中的位置示意图 Figure 6 Position of Loop 3, Loop 13 and active sites in the structure of mutant N210S/N211S/T212G. 球形部分为催化三联体(32D-63H-220S); 红色与棕色部分分别为活性位点63H与220S及其所在的α-螺旋; 橙色部分为活性位点32D及其所在的β-折叠; 黄色部分与蓝色部分分别为角蛋白酶的Loop 3与Loop 13 The catalytic triad residues (32D-63H-220S) are shown in spheres; The α-helix where the active site 63H located is shown in red; The α-helix where the active site 220S located is shown in brown; The β-sheet where the active site 32D located is shown in orange; The Loop 3 and Loop 13 of keratinase are shown in yellow and blue respectively. |
|
|
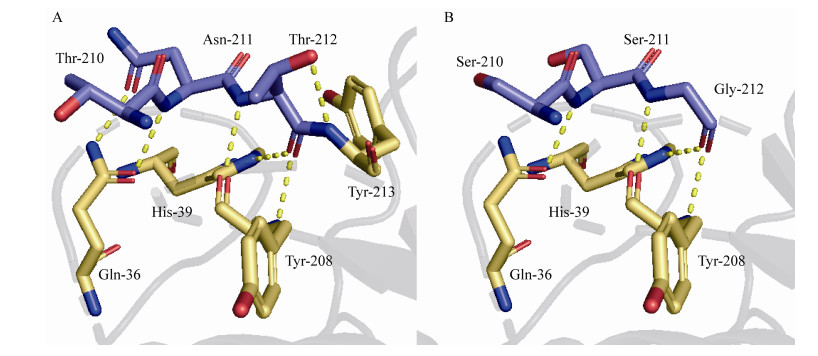
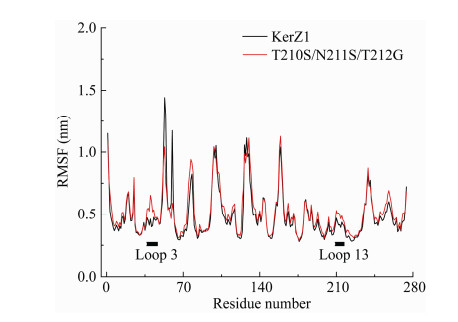
图 7为角蛋白酶KerZ1及其复合突变体在引入突变体前后的210–212位氨基酸与其他残基间氢键的示意图,野生酶的211N可与36Q形成2个氢键,其212T则分别与39H、208Y、213Y形成4个氢键(图 7A); 在引入突变T210S/N211S/T212G后,突变体211S与36Q形成的氢键减少了1个,而212G则不再与213Y形成氢键(图 7B),氢键的减少会降低酶分子解折叠需要的能量,提升酶分子的柔性。通过分子动力学模拟计算每个氨基酸残基的RMSF,以进一步揭示酶分子的灵活性[18],结果如图 8所示。相比KerZ1,在突变T210S/N211S/T212G引入后,整个loop 13显示出了更高的RMSF值,这说明复合突变的引入使得角蛋白酶在该loop区的灵活性得到了整体的提升。与此同时,与36Q残基氢键的减少也使得36Q所在的loop 3区域的RMSF得到提升,从而可能使得上述loop 3、loop 13及其相邻的β-折叠与角蛋白酶活性位点所在的α-螺旋及β-折叠组成的结构灵活性提升。由此推测,loop 3与loop 13间的氢键减少可能是揭示突变体T210S/N211S/T212G在低于最适温度下酶活提高的主要原因。除此之外,211N具有很强的亲水性,在突变为211S后其亲水性有显著的下降,表面疏水性的提升也会使分子柔性得到提升,从而使角蛋白酶的灵活性得到进一步的提高。
|
| 图 7 KerZ1 (A)及T210S/N211S/T212G (B)的三维结构及其氢键位置示意图 Figure 7 Three-dimensional structure and hydrogen bond position of KerZ1 (A) and T210S/N211S/T212G (B). |
|
|
|
| 图 8 KerZ1及T210S/N211S/T212G的残基灵活性比较 Figure 8 The residual flexibility of KerZ1 and T210S/N211S/T212G. |
|
|
为使角蛋白酶KerZ1适应工业生产和实际应用环境下的条件,本研究通过同源比对和对虚拟突变进行折叠自由能的分析,向角蛋白酶KerZ1中的柔性环区域引入氨基酸突变以提高其灵活性,进而提升角蛋白酶的低温催化活性。结果表明,对柔性环loop 13引入的3个氨基酸突变均使角蛋白酶KerZ1低温催化活性得到提升。对该柔性环进行复合突变并构建的突变体T210S/N211S/T212G与角蛋白酶KerZ1相比,其在柔性环loop 3及loop 13的灵活性得到了提高,并在中等温度和低温下均显示出更高的酶活力与催化效率。由于角蛋白酶结构较为复杂[27],因而本研究中仅对角蛋白酶在溶剂中的结构灵活性进行了初步分析。在下一步的研究中,将解析角蛋白酶在水解角蛋白过程中其底物分子对酶结构造成的影响,从而发掘潜在的角蛋白酶低温活性突变位点,并为进一步开发角蛋白酶提供理论基础。综上所述,本研究对嗜热角蛋白酶进行低温催化活性改造,有效地提高了枯草芽孢杆菌角蛋白酶在中等和低温条件下的催化活性,为提高其在工业应用中的实用性打下了基础,也为其他工业酶提供了较为新颖的改造思路。
| [1] |
Wang B, Yang W, Mckittrick J, Meyers MA. Keratin: structure, mechanical properties, occurrence in biological organisms, and efforts at bioinspiration[J]. Progress in Materials Science, 2016, 76: 229-318. DOI:10.1016/j.pmatsci.2015.06.001 |
| [2] |
Qiu JW, Wilkens C, Barrett K, Meyer AS. Microbial enzymes catalyzing keratin degradation: classification, structure, function[J]. Biotechnology Advances, 2020, 44: 107607. DOI:10.1016/j.biotechadv.2020.107607 |
| [3] |
De Oliveira Martinez J, Cai GQ, Nachtschatt M, Navone L, Zhang ZY, Robins K, Speight R. Challenges and opportunities in identifying and characterising keratinases for value-added peptide production[J]. Catalysts, 2020, 10(2): 184. DOI:10.3390/catal10020184 |
| [4] |
Verma A, Singh H, Anwar S, Chattopadhyay A, Tiwari KK, Kaur S, Dhilon GS. Microbial keratinases: industrial enzymes with waste management potential[J]. Critical Reviews in Biotechnology, 2017, 37(4): 476-491. DOI:10.1080/07388551.2016.1185388 |
| [5] |
Jaouadi NZ, Rekik H, Badis A, Trabelsi S, Belhoul M, Yahiaoui AB, Ben Aicha H, Toumi A, Bejar S, Jaouadi B. Biochemical and molecular characterization of a serine keratinase from Brevibacillus brevis US575 with promising keratin-biodegradation and hide-dehairing activities[J]. PLoS One, 2013, 8(10): e76722. DOI:10.1371/journal.pone.0076722 |
| [6] |
Sanghvi G, Patel H, Vaishnav D, Oza T, Dave G, Kunjadia P, Sheth N. A novel alkaline keratinase from Bacillus subtilis DP1 with potential utility in cosmetic formulation[J]. International Journal of Biological Macromolecules, 2016, 87: 256-262. DOI:10.1016/j.ijbiomac.2016.02.067 |
| [7] |
Hou YH, Ding HB. Research progress on keratinase and its applications in feed industry[J]. Chinese Journal of Animal Science, 2018, 54(1): 13-18. (in Chinese) 侯玉煌, 丁宏标. 角蛋白酶研究进展及其在饲料工业中的应用[J]. 中国畜牧杂志, 2018, 54(1): 13-18. |
| [8] |
Peng Z, Mao XZ, Zhang J, Du GC, Chen J. Biotransformation of keratin waste to amino acids and active peptides based on cell-free catalysis[J]. Biotechnology for Biofuels, 2020, 13(1): 1-12. DOI:10.1186/s13068-019-1642-1 |
| [9] |
Siddiqui KS. Some like it hot, some like it cold: temperature dependent biotechnological applications and improvements in extremophilic enzymes[J]. Biotechnology Advances, 2015, 33(8): 1912-1922. DOI:10.1016/j.biotechadv.2015.11.001 |
| [10] |
Nandanwar SK, Borkar SB, Lee JH, Kim HJ. Taking advantage of promiscuity of cold-active enzymes[J]. Applied Sciences, 2020, 10(22): 8128. DOI:10.3390/app10228128 |
| [11] |
Siddiqui KS. Defying the activity-stability trade-off in enzymes: taking advantage of entropy to enhance activity and thermostability[J]. Critical Reviews in Biotechnology, 2017, 37(3): 309-322. DOI:10.3109/07388551.2016.1144045 |
| [12] |
Struvay C, Feller G. Optimization to low temperature activity in psychrophilic enzymes[J]. International Journal of Molecular Sciences, 2012, 13(9): 11643-11665. |
| [13] |
Sasaki M, Uno M, Akanuma S, Yamagishi A. Random mutagenesis improves the low-temperature activity of the tetrameric 3-isopropylmalate dehydrogenase from the hyperthermophile Sulfolobus tokodaii[J]. Protein Engineering, Design and Selection, 2008, 21(12): 721-727. DOI:10.1093/protein/gzn054 |
| [14] |
Hu YC, Li T, Tu Z, He QH, Li YP, Fu JH. Engineering a recombination neutral protease I from Aspergillus oryzae to improve enzyme activity at acidic pH[J]. RSC Advances, 2020, 10(51): 30692-30699. DOI:10.1039/D0RA05462C |
| [15] |
Zhao HY, Feng H. Engineering Bacillus pumilus alkaline serine protease to increase its low-temperature proteolytic activity by directed evolution[J]. BMC Biotechnology, 2018, 18(1): 34. DOI:10.1186/s12896-018-0451-0 |
| [16] |
Okai M, Onoue C, Tsuda R, Ishigami C, Yoshida-Mishima C, Urano N, Kato C, Ishida M. Q301P mutant of Vibrio PR protease affects activities under low-temperature and high-pressure conditions[J]. Journal of Bioscience and Bioengineering, 2020, 130(4): 341-346. DOI:10.1016/j.jbiosc.2020.05.011 |
| [17] |
Sugii T, Akanuma S, Yagi S, Yagyu K, Shimoda Y, Yamagishi A. Characterization of the low-temperature activity of Sulfolobus tokodaii glucose-1-dehydrogenase mutants[J]. Journal of Bioscience and Bioengineering, 2014, 118(4): 367-371. DOI:10.1016/j.jbiosc.2014.03.002 |
| [18] |
Zhang R, He LM, Shen JD, Miao Y, Tang XH, Wu Q, Zhou JP, Huang ZX. Improving low-temperature activity and thermostability of exo-inulinase InuAGN25 on the basis of increasing rigidity of the Terminus and flexibility of the catalytic domain[J]. Bioengineered, 2020, 11(1): 1233-1244. DOI:10.1080/21655979.2020.1837476 |
| [19] |
Kumar V, Yedavalli P, Gupta V, Rao NM. Engineering lipase A from mesophilic Bacillus subtilis for activity at low temperatures[J]. Protein Engineering, Design and Selection, 2014, 27(3): 73-82. DOI:10.1093/protein/gzt064 |
| [20] |
Derache C, Epinette C, Roussel A, Gabant G, Cadene M, Korkmaz B, Gauthier F, Kellenberger C. Crystal structure of greglin, a novel non-classical Kazal inhibitor, in complex with subtilisin[J]. The FEBS Journal, 2012, 279(24): 4466-4478. DOI:10.1111/febs.12033 |
| [21] |
Miao ZD. Modification the thermostability of Bacillus subtilis keratinase[D]. Wuxi: Master's Thesis of Jiangnan University, 2021 (in Chinese) 苗周迪. 枯草芽孢杆菌角蛋白酶热稳定性的改造[D]. 无锡: 江南大学硕士学位论文, 2021 |
| [22] |
Lv LX, Sim MH, Li YD, Min J, Feng WH, Guan WJ, Li YQ. Production, characterization and application of a keratinase from Chryseobacterium L99 sp. nov.[J]. Process Biochemistry, 2010, 45(8): 1236-1244. DOI:10.1016/j.procbio.2010.03.011 |
| [23] |
Ó'Fágáin C. Enzyme stabilization — recent experimental progress[J]. Enzyme and Microbial Technology, 2003, 33(2/3): 137-149. |
| [24] |
Su C, Gong JS, Sun YX, Qin JF, Zhai S, Li H, Li H, Lu ZM, Xu ZH, Shi JS. Combining pro-peptide engineering and multisite saturation mutagenesis to improve the catalytic potential of keratinase[J]. ACS synthetic biology, 2019, 8(2): 435-433. |
| [25] |
Tian J, Wang P, Wu NF, Fan YL. Recent advances in the rational design to improve the protein thermostability[J]. Current Biotechnology, 2012, 2(4): 233-239. (in Chinese) 田健, 王平, 伍宁丰, 范云六. 理性设计提高蛋白质热稳定性的研究进展[J]. 生物技术进展, 2012, 2(4): 233-239. DOI:10.3969/j.issn.2095-2341.2012.04.01 |
| [26] |
Tong LM, Liu S, Li JH, Du GC, Chen J. Improvement of TGase thermal stability through site-directed mutagenesis based on analysis of folding free energy[J]. Journal of Food Science and Biotechnology, 2018, 37(12): 1278-1283. (in Chinese) 童理明, 刘松, 李江华, 堵国城, 陈坚. 基于蛋白质折叠自由能分析的定点突变提高谷氨酰胺转胺酶热稳定性[J]. 食品与生物技术学报, 2018, 37(12): 1278-1283. |
| [27] |
Jia RY, He YF, Wang RM, Li FR, Wang Y. Advanced in structure, extract and applications of keratins[J]. Chemistry, 2008, 71(4): 265-271. (in Chinese) 贾如琰, 何玉凤, 王荣民, 李芳蓉, 王艳. 角蛋白的分子构成、提取及应用[J]. 化学通报, 2008, 71(4): 265-271. |
 2022, Vol. 49
2022, Vol. 49